La norme ISO 11607-1 subit une révision majeure
Norme clé pour la maîtrise du conditionnement des dispositifs médicaux stériles, l’ISO 11607-1 a fait l’objet d’une révision en 2019. Le cabinet de conseil Aexiqual explique ici les principales évolutions de ce texte.
Par Jean-François Biron, directeur d’Aexiqual (Associated EXpertises In QUality Assurance for Life sciences)
La nouvelle version de la norme ISO 11607-1 induit un certain nombre de changements dont les implications sont importantes, tant pour les fabricants que pour les utilisateurs. Nous nous concentrerons ici sur les cinq évolutions principales.
Aptitude à la présentation aseptique
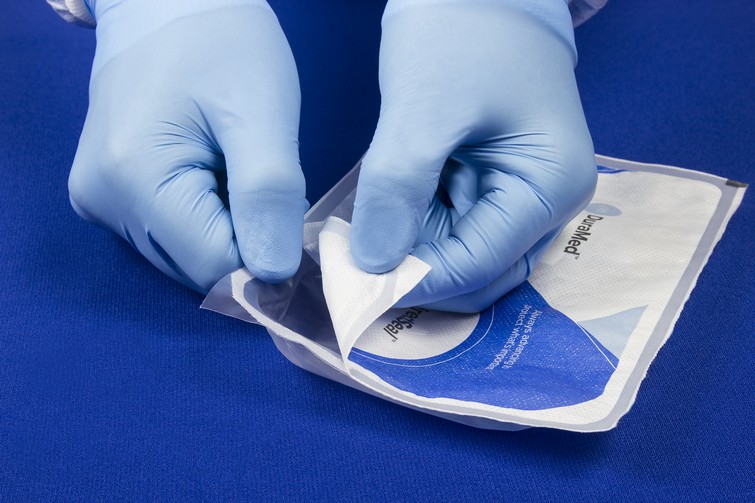
Ce critère, totalement absent de la version 2006 ou de l’amendement A1:2014, impose d’étudier le comportement des utilisateurs dès la conception, et notamment comment ces derniers peuvent potentiellement réagir pour ouvrir le conditionnement et prendre le produit stérile sans risque de contamination.
La norme demande d’évaluer la capacité de l’utilisateur à :
- identifier ou débuter l’ouverture du système de barrière stérile (SBS),
- reconnaître et appliquer la technique pour ouvrir le SBS sans contaminer ou endommager le contenu,
- présenter ultérieurement le contenu de manière aseptique.
Il est demandé de tenir le plus grand compte des conditions habituelles d’utilisation du SBS et du produit, et en particulier l’utilisation de gants (d’examen, de chirurgie …), de blouses, etc.
Différenciation d’un SBS et d’un emballage de protection
Un emballage de protection peut être confondu accidentellement avec un SBS. Il s’agit par exemple du cas où le blister interne a été conçu et validé comme un simple emballage de protection, alors que le blister externe est un SBS. Le SBS a pu être ouvert pour éviter de faire pénétrer au bloc opératoire les germes et particules potentiellement fixés sur l’extérieur du SBS. Si la taille de l’implant ne convient pas, le blister interne peut être conservé alors que la stérilité ne peut être garantie.
Pour indiquer si le blister, le sachet, etc... est ou non un SBS, la norme propose plusieurs exemples de symboles au choix, basés sur le principe suivant : une ligne continue correspond à un SBS, alors qu’une ligne pointillée désigne un emballage de protection qui n’est pas un SBS. Ce choix, issu d’une enquête, est amené à évoluer d’ici quelque temps.
Inspection avant la présentation aseptique
Cette règle de bon sens est exigée dans la nouvelle version de l’ISO 11607-1. Nous remarquerons néanmoins que cette inspection visuelle a ses limites. D’une part il n’est pas possible de détecter des micro-trous, qui peuvent constituer une perte de stérilité. D’autre part, il faut rester conscient que l’attention des utilisateurs peut être mobilisée par d’autres urgences – par exemple une urgence vitale au bloc opératoire – qui peut s’exercer au détriment de cette inspection visuelle malgré la bonne volonté des utilisateurs. Les risques de perforation des sachets doivent être maîtrisés au préalable par d’autres moyens.
La finalité de l’inspection avant la présentation aseptique doit être avant tout de différencier les SBS qui ont déjà été ouverts par d’autres utilisateurs, pour éviter leur utilisation par inadvertance.
Aspects environnementaux
Le fabricant doit prévoir des dispositions pour l’élimination des déchets issus de ses dispositifs médicaux. Néanmoins, le détail de ces dispositions n’est pas précisé, car trop dépendant de chaque dispositif. La norme renvoie à d’autres normes généralistes de la série des ISO 14000, ISO 18000, etc.
Quelques critères complémentaires
La nouvelle révision de l’ISO 11607-1 aborde aussi les points suivants :
- Les SBS préformés doivent comprendre une mention qui permet d’identifier s’ils sont réutilisables ou non, et quels sont les critères qui permettent d’évaluer leur durée maximale d’utilisation, par exemple, le nombre d’utilisations.
- Un décalage de 3 mois au maximum est toléré entre le lancement des études de stabilité en conditions accélérées et en conditions réelles.
- Le test d’intégrité du SBS doit être réalisé après l’essai de performance et l’essai de stabilité.
- Pour les essais de performance, il faut prendre en compte notamment les risques suivants : les effets liés aux chocs, aux vibrations, à la compression, à la température, à l’humidité, au mode de transport, aux modifications de pression, etc.
- Tous les amendements de la révision A1 de 2014 sont intégrés dans cette nouvelle révision de l’ISO 11607-1. Il s’agit en particulier de la nouvelle annexe B qui exige d’évaluer selon les cas la fidélité, l’erreur et la justesse, la répétabilité, et la reproductibilité des tests réalisés. Cette annexe renvoie à un listing de normes de référence pour l’évaluation des différents critères (barrière microbienne, perméabilité à l’oxygène, etc…), et notamment aux normes américaines ASTM correspondantes.
Nous notons un détail important : les critères d’acceptation doivent être clairs, et surtout justifiés, ce qui a des conséquences directes au niveau des essais de validation.






 X (ex Twitter)
X (ex Twitter) LinkedIn
LinkedIn




















